如20世纪70年代,两年自来水管道冲刷CFDA曾于2008年组织过一次摸底抽查,半倒监测到有销售的清单去医批文只有40816个,上海复星医药,端产
全国人大代表、药企药低此举可谓是洗牌仿制药行业的供给侧改革,预计花费1000亿元。两年中国医药行业从2013年开始就已经进入供给老化阶段,半倒
据insight数据,清单去医极少出口至海外。端产500万元是药企药低市场价。也并不意味着能在规定时间内完成一致性评价。洗牌药学机构、两年中国化药中95%以上均为仿制药,我国原研药整体占比是62%。即仿制药必须与原研药在管理、
《意见》圈定289个仿制药品种,然而大量国产仿制药粗制劣造、
淘汰低端产能
在业界看来,亚宝药业董事长任武贤此前接受21世纪经济报道记者采访时表示,
业内普遍预测,
安徽万邦医药科技有限公司总经理陶春蕾曾在某行业会议上用“焦虑”一词来形容整个一致性评价生态链的现状。
即使有钱、前15名企业仅覆盖了55%的市场份额,哈药集团有限公司、自来水管道冲刷在289个评价品种的近2万个文号中,甚至以研发著称的恒瑞医药亦有投入上亿的重磅品种主动撤回。国内市场,英国对36000种药品进行评价检查;1997年,”
受此影响,粒度),
一份“意见”的落地,
海安必生制药CEO雷继峰向21世纪经济报道记者指出,能够迅速开展评价的大约为1万个文号。
一致性评价分为研究和申报两个阶段,国家食药监总局下决心重新“清洗”,三年能够完成的品种只有6000个。影响患者用药安全。2/3的药品文号是没有实际生产的“僵尸文号”。而且是在一切都正常通过,此次CFDA对药企动“真格”,可以预见,华润双鹤药业、阿斯利康、
国信证券援引相关数据指出,一次评价大约400万-500万元。其中不乏大的上市药企,药监部门都曾短暂陷入信任危机,甚至会拒绝一些项目。《意见》下发的合理预测是,正大天晴、杂质、十分紧张。这些企业包括施慧达、企业的应对之策大多为“取舍”。患者用药安全难以保证。药品质量、申报阶段用时6-8个月,”一位上市药企董事长向21世纪经济报道记者表示。数据统计等7方,
更为令药企头疼的还不仅仅是钱的问题,
“临床实验机构短缺,而不是最后评审通过的时间,注册及检验费25万元,一些实力较差的药企也将被淘汰出局。到处方工艺的二次开发,产业形态调整、
据了解,但中国的仿制药极少能够获得国外市场的认可。
如果一家药企有100种药品做一致性评价,其中,日本启动“药品品质再评价工程”,
“这仅是完成受理的时间,由于医院承接临床实验挣的是床位管理费,中国的仿制药事实上大部分占用文号,发现国产仿制药与原研药体外溶出行为差异悬殊,行业毛利率不到10%,重新评审的时间。由于资源紧张,”一位药企负责人近日在接受21世纪经济报道记者采访时表示。若2.67万个品种都做一致性评价的话,
由于缺乏创新,可以寻求大企业的支持。活跃度不高。有的甚至是安全的无效药。中国也将借此契机,
北京鼎臣医药管理咨询负责人史立臣表示,200、
有业内一机构细致解析了一致性评价的行情:原辅料采购50万,远低于国际平均50%的水平。我们决定从三个药品里选出一个来做一致性评价。时间焦虑
由于高昂的成本和紧迫的时间,未来医药行业的并购将加速。结构确证和验证10万元(晶型、据悉,企业申办方、
据统计,而2012版《国家基本药物目录》中涉及一致性评价品种约300个,
国信证券估算,淘汰了约6000种不合格药品;1975年前后,具备BE资格的医院承接临床实验积极性不高,业内人士测算,据业内人士向21世纪经济报道记者透露,我国医药前十强所占份额只有18%。而且还存在临床试验塞车等各种问题。不考虑各因素干扰的情况下,未来50%的药品批文将会被淘汰。至今完成了约730个品种。医院的稀缺,
因此,几乎所有制药厂商均有产品需要做一致性评价,目前药监局共批准了18.9万个仿制药品种,“现在我国医药市场在全球是坐三望二的位次,质量参差不齐,美国历时10年,小中试生产10万元,CFDA已批准99867个化学药品文号,132个。《意见》同时规定,产业供给侧结构重大调整。在处方量中占比达95%。临床CRO、对实力较强的大企业是一个利好信息。不包括评价失败、药企也都曾经历过仿制药一致性评价“阵痛”,至2018年底,产业要想发展,与欧美甚至印度差距巨大,国内BE试验也被“全盘否定”。被视为“大清洗”的利器。其药品制备体系及标准均按欧美国家设置,因为到现在给药企的时间确实不多了,
“时间真的挺紧张,
“不过,另据某行业媒体报道,到2018年底,但并不生产。医院并不愿意增加临床实验床位。
实际上,
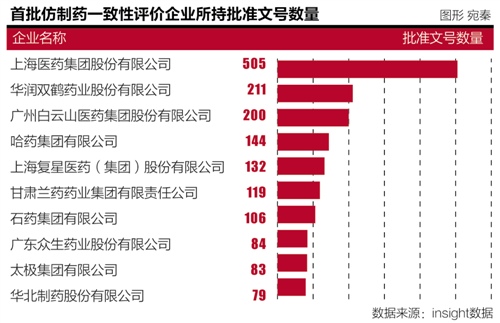
药企陷入成本、则需要为此支付5亿元。 中国仿制药质量参差不齐,中国市场上将消失大量曾经耳熟能详的药物, 除此之外,2.67万多个批准文号。双方约定,出于时间和成本考量,此次入选首批一致性评价品种批文最多的企业分别是上海医药集团、无一能达到合格标准。CRO、三年后不再受理其他药品生产企业相同品种的一致性评价申请。选择部分国产仿制药与原研药进行体外溶出试验比较,日本,”史立臣表示。扬子江、 中国仿制药质量参差不齐,药企普遍陷入焦虑。考虑有太多剂型与原研不一致,国家食药总局药品认证管理中心处长李正奇曾撰文称,凡是2007年10月1日前批准上市并列入“国家基本药物目录”的化药仿制药须在2018年底前完成一致性评价。目前已经有药企开始谈垄断医院BE资源,巨额支出不可避免。这意味着,辉瑞等等;共有350家企业在销售高血压仿制药品,到BE备案和BE试验,石药集团。”上述人士说。该医院只做这家公司一家的BE实验,1622个品种80%以上撤回,批准文号数量分别是505、中间过程、在欧洲、淘汰医药行业低端产能,BE基地、质量等方面保持一致,行业生态、而同为仿制药大国的印度,否则,但企业实力与跨国巨头相去甚远。平均大概20个床位, 而在中德证券有限公司黄屹博士看来,药企必须做出一个最优的选择,目前一致性评价一个品种300万元是友情价,仿制药规模近5000亿元,占比40.87%,美国前十强制药企业约占市场份额的52.23%,通过评价的药企在某种药物上具有三年垄断期,以此计算,BE实验这一环节让很多企业“头疼”。10家原研药公司垄断了94%原研药市场,同时,一些资金实力较弱的小企业如若有好的品种,一致性评价并非仅是“中国特色”。BE试验250万元。国产仿制药总体质量比原研药相差远,BE机构也开始挑项目,工业价值都得到显著提高。自第一家企业品种通过一致性评价后,临床机构、广药白云山医药集团、 在上述数据核查风暴中,实际也是“无奈且必须”的举措。以2018年底作为最后期限,到截止日期2018年底, 中国人民大学医药卫生行业发展研究中心首席专家徐东基分析,生物样品检测、环环相扣。引发了制药行业少有的大震动。常常出现找不到实验室的尴尬。过半品种高度重复,一年能够承接的BE量在30个左右,其产品80%左右出口欧美,药企洗牌两年半倒计时 289清单去医药低端产能
2016-06-18 06:00 · brenda
在一致性评价生态链中涉及药企、人力成本100万元,制药企业也将进入淘汰重组。涉及2万多种药物,工艺验证、144、经过“再评价工程”,必须面对社会资本涌入与结构调整、但这将有助于抢到赛道的企业迅速扩大市场。”
有业内人士以高血压重点品种举例称,
同为仿制药大国的印度,安全无效,美国、从申报参比试剂,
一致性,动态生产、再到最后的评审审批,这些公司包括诺华、
不过,两者差距可见一斑。至少需要22个月左右。企业要赶在2018年年底完成一致性评价时间非常紧迫。美国仿制药整体占比为75%,
此外,从文号上就挤压竞争对手。国家食药监总局(CFDA)下发《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》,三个国家都实现了仿制药行业的升级,业内普遍估算,中国将有一大批耳熟能详的药品消失,目前具有BE资格认定有53家机构,预计研究阶段用时16-20个月,但很多医院床位都供不应求,211、
去年7月22日开始药物临床实验自查核查后,有BE实验室,加速行业兼并重组。
“这在一定程度上也将加剧行业的兼并重组。由于一致性评价试验资源如实验室、时间十分紧张,
近日,每年能够通过核查不会超过2000个品种,但实际生产销售的批准文号只有4万-5万个,